知识分享|解读-ISO 11737-1-2018 保健品灭菌.微生物学方法.第1部分:产品上微生物群落的测定
ISO 11737-1 2006版距今已经12年了,其内容和方法与目前的技术发展已经有了很大的变化。在这样的背景下,ISO11737-1第三版由ISO/TC 198医疗保健产品灭菌技术委员会于2018年1月正式发布。标准的主题不变,仍旧是关注医疗保健产品上活的微生物计数和鉴定方法,用于确定产品、零部件、原材料或包装中微生物的数量。
本标准不适用于环境中的微生物检测,也不适用于病毒、朊病毒或原生动物的污染物检测,关于病毒和朊病毒的杀灭可以参考ISO 22442-3、ICH Q5A (R1)和ISO 13022中的方法。
目前网络上还没有对新标准的解读,甚至老版本标准的解读都很少。但这个标准其实对于医疗产品的微生物检测方法是很好的指南,对于需要灭菌的产品也是确定灭菌方法的关键因素。对比上一版本,ISO 11737-1 2018版的主要变化如下:
1. 引入了“Bioburden spikes”的术语,作为生物负载正常和一致性的部分,并提供了数据的举例;
根据bioburden spike的定义来看,是指单个的生物负载数值极大地高于一系列其他的数据,形成一个尖峰。出现这种现象时,可能有以下两种情况,需要判断其是否为产品的一致表现,并评估其影响。
该值不是生物负载分布的正常和一致的部分,这时需要调查制造过程、微生物测试以及样品的处理流程,以寻找可能的失误;
通过回顾历史数据发现,该值可能是生物负载分布的正常和一致的部分,历史数据表明一个较大的值会定期出现,并且微生物的种类相同,这样就使其成为生物负载的一致组成部分。这些尖峰应该在灭菌过程的处理程度上得到考虑,例如一个生物负载的尖峰出现可能是由于原材料的不稳定,或者加工过程引入了过多的处理。
2. 澄清了包装一般不会进行微生物测试,除非包装作为产品整体的一部分;
在进行产品的微生物检测时,产品应处于正常的包装中。一般情况下,是可以将产品从包装系统中取出并进行生物负载测试的,也就是忽略其包装系统对于生物负载的贡献。但基于无菌标签的声明,内包材如吸塑盒或产品说明书在如下情况下可能也需要纳入生物负载的测试:
哪些组成部分预期是无菌的;
当包装是产品整体的一部分时;
用于特定的评估目的
个人认为标准还是强调了包装系统对于生物负载是有影响的,如果整个产品的无菌包装系统内含有另外的包装材料,那么这些包装材料是需要进行微生物检测的(如吸塑盒中用于缓冲的泡沫衬垫);双层无菌包装中的内包装也要进行相应的微生物测试。
3. 提供了更多关于最大可能数量(most probablenumber, MPN)技术的信息和其应用;
最大可能数量一般用于产品上的微生物分布随机且平均值较小的情况,如液态、粘性流体或粉末状的产品,而且MPN方法适用于微生物水平的一般评估,而不是精确测定。
4. 提供了改善检测限(limit of detection, LOD)方法的细节和数据的正确使用;
在微生物报告中,当产品的浸提液的一部分被用于检测微生物,并且得到的结果为0个菌落时,最终的结果一般会表示为小于X,其中1/X是浸提液用于检测的比例。例如当一个产品的浸提液为400ml时,取1/4进行过滤,得到0个菌落,最终报告上会写明<4 CFU,因此该方法的检测限为4,<4 CFU意味着整个产品上可能会含有0, 1, 2, 或3 CFU,但微生物报告的规则要求其表示为<4 CFU。
单个的微生物结果一般为整数,因为其代表了菌落的数量;多个数据的平均值或其他数学计算结果一般取一位小数。检测限可以通过以下方法得到改善:
对测试方法的改善(例如过滤更多比例的浸提液);
使用多个产品为一组进行检测;
使用其他测试方法,如MPN法。
5. 删除了部分关于生物负载数据评估的统计学方法讨论,原因是这部分信息并不具备代表性或不需要;
新标准中的A.8.8统计方法部分删除了上一个版本中使用变换技术使数据的分布变得对称和对偏态分布适用的统计学技术。还删除了表明样本量和生物负载波动之间关系的统计学表格A.3。
6. 增加了选择生物负载回收率方法的准则表格,解释了校正因子(correctionfactor, CF)的使用,删除了回收率<50%时需要技术修正的要求;
校正因子(CF)是针对无法完全浸提产品上的微生物,或者无法完全培养出浸提到的微生物的情况,用于补偿计算数值的一种方式。通常进行生物负载的回收率测试来得到校正因子,使结果更加接近真实的微生物数量。回收率测试一般有两种方法:重复回收和产品接种。考虑选择哪种方式的主要因素是产品上微生物的水平。
通常重复回收法适用于产品上微生物数量较多的情况,产品接种法适用于产品上微生物数量较少的情况。回收率结果和对应的校正因子会随着微生物浸提参数的不同而变化(如重复回收的类型和次数,或者不同的回收率测试方法)。因此,需要考虑确定回收率的目的和相应微生物数据收集的目的。
老版本标准中对于回收率<50%时需要进行技术的改善,使回收率提高到50%以上。新版标准中移除了这个要求,由于不同的设计、材料、产品类型、加工工艺等,标准不要求达到某一特定的回收率。但是如果回收率没有达到预期的指标,应尝试另一种技术来确定是否可以提高回收率。有时回收率由于某些情况无法达到50%以上也是可以接受的(如某可吸收或特别复杂的产品回收率20%也可以接受)。也要注意某些情况下确定产品的回收率也是不必要的(如子件或原材料的筛选,或某液体产品且其全部组成均被过滤)。
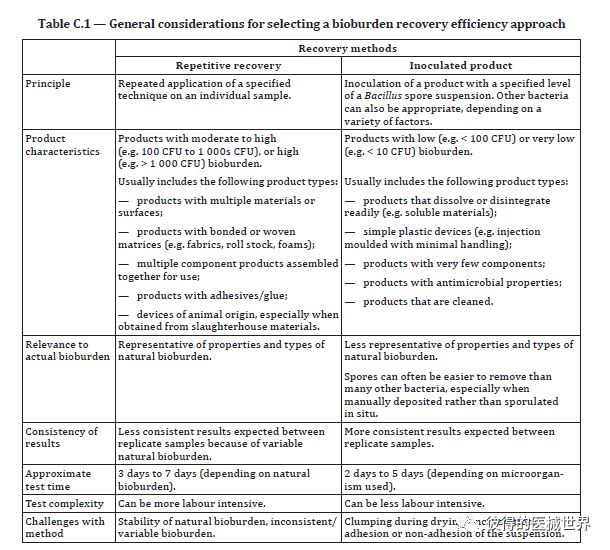
附表C.1-选择生物负载回收率方法的一般考量
7. 提供了更多关于生物负载方法适用性测试的信息;
生物负载的方法适用性测试用于证明产品不会抑制微生物的生长或检测。由于产品上可能会含有抑制微生物生长的物质(如抗生素等),可以通过稀释或中和的方法来降低这些抑制因素。当有新产品或者产品发生变更时,或者测试条件发生变化时(如培养条件,浸提介质等),需要进行生物负载的方法适用性测试。
8. 增加了一个章节,用于详细描述直接平板计数、估计计数和超出理想范围的计数规则;
标准的A.8.2.2对平板计数的方法进行了说明。通常微生物计数方法中推荐选择合适的平板进行计数(例如小于200CFU,25到250CFU,或者30到300CFU),这适用于进行了多次稀释的情况,来选择合理的稀释倍数。但有些情况下,如产品本身含有较少的微生物,由于数量较低不能进行多次稀释。在这些情况下,可以选择较少菌落的平板进行直接计数。
平板计数可以有三种方法:
直接计数:即直接读取平板上的菌落数;
估计读数:即读取平板上一部分的菌落数,然后按照比例推算整个平板上的菌落数量。这种方法也适用于平板上有菌落弥漫成片但还有菌落可计数的情况;
超出可读或可估计的范围的计数:可以尝试半定量的方式来进行推算,如果实在无法推算,应定义结果为TNTC(too numerous to count),TNTC的结果应予以调查。
9. 增加了关于澄清制造商和实验室之间责任的表格;
新版标准专门增加了Annex D,对于制造商和实验室之间责任的划分做了澄清。制造商和实验室之间应有协议来划分职责,最终制造商应负责确保标准的要求得到满足。附录D对典型的职责划分做了描述。
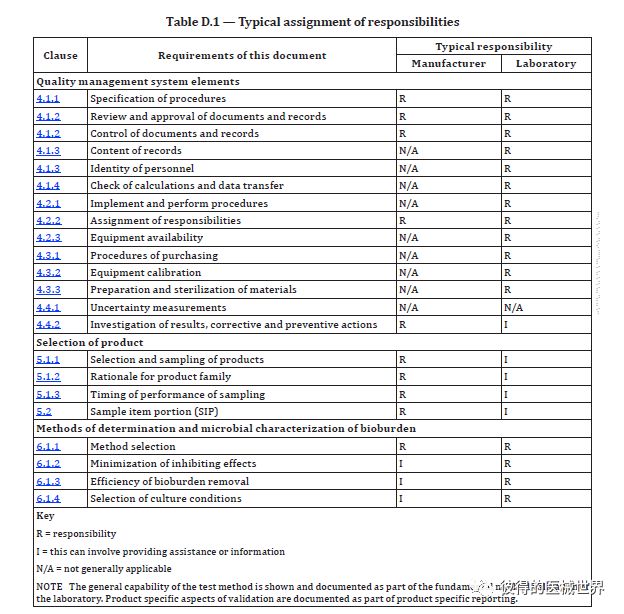

附表D.1-典型的责任划分
10. 增强了关注基于风险的方法,包括生物负载数据使用的目的。
ISO 11737-1 2018版本的变化很大,多数是汲取了行业内的最新技术水平和理解(state-of-the-art),为医疗产品的微生物检测提供了详细而有效的指南,希望本文对各位理解新版标准,了解最新动态有所帮助。
【本文来源: 彼得的医械世界】

全部 0条评论