1 回答
GB9706.1(医用电气设备安全通用要求)是以预防或减少医疗器械的能量危害为主要目标的通用安全要求标准,主要章节包含有对电击危险、机械危险、辐射危险、超温危险等的防护,在新版GB9706.1中又增加了大量风险管理的内容,是医用电气设备生产企业普遍遵守的通用标准。并列标准中,YY 9706.102(电磁兼容)、YY/T 9706.106(可用性)适用于所有医用电气设备;其他并列标准适用于具有辐射防护、报警、家用、急救、生理闭环控制器等特定功能或预期用途的医用电气设备。专用标准涉及医用X线、医用超声、放射治疗、物理治疗、医用光学、齿科、体外循环、呼吸麻醉、医用电子仪器等9个领域51类产品。另外,新版系列标准正在制修订的项目还有17项(包括国标6项,行标11项),均为专用标准。
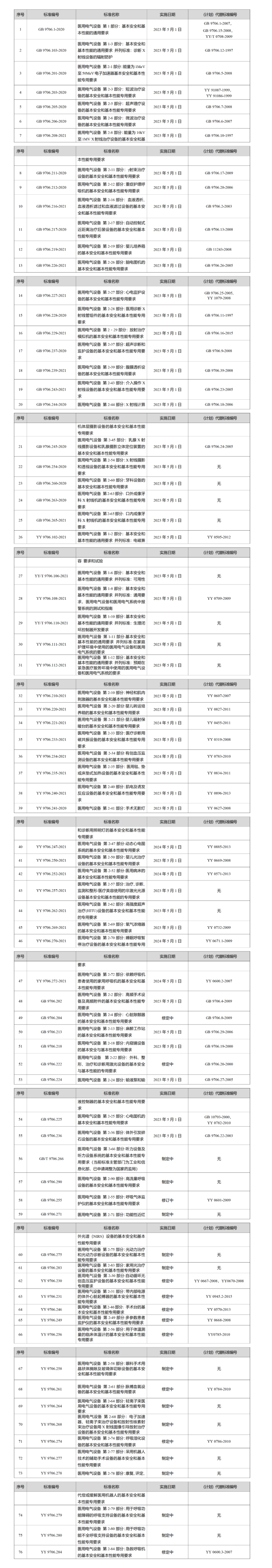
GB 9706.1-2020及配套并列、专用标准信息表